injektionsvätska, suspension i förfylld spruta
Polysackaridvaccin mot pneumokockinfektioner, konjugerat, adsorberat
natrium
Källa: Fass.se
Bipacksedel: Information till användaren
injektionsvätska, suspension i förfylld spruta
Polysackaridvaccin mot pneumokockinfektioner, konjugerat, adsorberat
natrium
Spara denna information, du kan behöva läsa den igen.
Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
Detta vaccin har ordinerats enbart åt ditt barn. Ge det inte till andra.
Om ditt barn får biverkningar tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt 4.
Synflorix är ett vaccin mot pneumokockinfektioner. En läkare eller sjuksköterska kommer att injicera ditt barn med detta vaccin.
Det används från 6 veckor upp till 5 års ålder för att skydda ditt barn mot:
en bakterie som kallas för ”Streptococcus pneumoniae”. Denna bakterie kan orsaka allvarliga sjukdomar, bland annat hjärnhinneinflammation, blodförgiftning och bakteriemi (bakterier i blodbanan) såväl som öroninfektion eller lunginflammation.
Hur Synflorix fungerar
Synflorix hjälper kroppen att producera egna antikroppar. Antikroppar är en del av det immunsystem som kommer att skydda ditt barn mot dessa sjukdomar.
ditt barn är allergiskt mot de aktiva substanserna eller mot något av övriga innehållsämnen i detta vaccin (innehållsämnena anges i avsnitt 6). Tecken på en allergisk reaktion kan bland annat vara kliande hudutslag, andfåddhet och svullnad av ansikte eller tunga.
ditt barn har en allvarlig infektion med hög feber (över 38°C). Om så är fallet kan vaccinationen skjutas upp tills ditt barn mår bättre. En lindrig infektion som en förkylning bör inte vara något problem. Tala dock först med läkaren.
Synflorix bör inte ges om något av ovanstående gäller för ditt barn. Om du är osäker, tala med läkare eller apotekspersonal innan ditt barn får Synflorix.
Kontrollera med läkare eller apotekspersonal innan detta vaccin ges om:
ditt barn har problem med blödningar eller lätt får blåmärken.
Hos barn från 2 års ålder kan svimning förekomma efter, eller även före, all nålinjektion. Tala därför om för läkaren eller sjuksköterskan om ditt barn har svimmat vid tidigare injektion.
Som för alla vacciner uppnås eventuellt inte fullt skydd hos alla barn som vaccineras med Synflorix.
Synflorix skyddar endast mot infektioner som orsakas av de bakterier för vilka vaccinet har utvecklats.
Barn med nedsatt immunförsvar (t.ex. på grund av infektion med humant immunbristvirus (hiv) eller immunsuppressiv behandling) får eventuellt inte full nytta av Synflorix.
Om du är osäker, tala med läkare eller apotekspersonal innan ditt barn får Synflorix.
Barn över 5 år
Vaccinets säkerhet och effekt har inte fastställts för barn som är äldre än 5 år och därför rekommenderas inte vaccination av dessa barn.
Tala om för läkare eller apotekspersonal om ditt barn tar, nyligen har tagit eller kan tänkas ta andra läkemedel, eller om barnet nyligen fått något annat vaccin. Synflorix fungerar eventuellt inte lika bra om barnet tar läkemedel som påverkar immunsystemets förmåga att bekämpa infektioner.
Synflorix kan ges samtidigt med andra barnvacciner såsom vaccin mot difteri, stelkramp, kikhosta (pertussis), Haemophilus influenzae typ b, polio (oralt eller inaktiverat), hepatit B, mässling-påssjuka-röda hund, vattkoppor, rotavirus (oralt) samt även meningokock serogrupp C och serogrupp A, C, W-135, Y (konjugerat). Olika ställen används för injicering av de olika vaccinerna.
Läkaren kan eventuellt be dig att ge barnet ett febernedsättande läkemedel (som till exempel paracetamol) innan eller direkt efter att Synflorix ges, i synnerhet om barnet samtidigt med Synflorix vaccineras med helcellsvaccin mot kikhosta. Febernedsättande läkemedel rekommenderas också till barn som har krampsjukdomar eller som tidigare haft feberkramper.
Om ditt barn har fått paracetamol före eller direkt efter att Synflorix har givits kan den erhållna nivån av antikroppar minska något. Det är inte känt om den minskade antikroppsnivån påverkar skyddet mot pneumokocksjukdomar.
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos, det vill säga är näst intill ”natriumfritt”.
Hur vaccinet ges
Synflorix injiceras alltid i en muskel. Detta görs vanligtvis i låret eller i överarmen.
Hur mycket ges
Vanligtvis får ditt barn (från 6 veckor till 6 månaders ålder) en vaccinationsserie omfattande 4 injektioner enligt officiella rekommendationer eller annan dosering enligt officiella rekommendationer som följs av sjukvårdspersonalen. Det är viktigt att följa läkarens eller sjuksköterskans instruktioner för att fullfölja vaccinationsschemat.
Varje injektion ges med minst en månads mellanrum, förutom den sista injektionen (booster) som ges minst 6 månader efter den tredje injektionen.
Den första injektionen kan ges från 6 veckors ålder och uppåt. Den sista injektionen (booster) kan ges från 9 månaders ålder och uppåt.
Du kommer att få veta när ditt barn ska komma tillbaka för nästa vaccination.
För tidigt födda barn (födda efter 27 veckors och innan 37 veckors graviditet):
Ditt barn (från 2 månader till 6 månaders ålder) kommer att få 3 injektioner med ett intervall på minst en månad mellan varje dos. Minst sex månader efter den sista injektionen kommer ditt barn få en ytterligare dos (boosterdos).
Spädbarn i åldern 7 till 11 månader kommer att få 2 injektioner. Varje injektion kommer att ges med minst en månads mellanrum. En tredje injektion (booster) kommer att ges under andra levnadsåret med minst två månaders mellanrum.
Barn från 12 månader till 5 års ålder kommer att få 2 injektioner. Varje injektion ges med minst två månaders mellanrum.
Särskilda patientgrupper
Barn från 6 veckor upp till 5 års ålder som anses ha högre risk att få pneumokockinfektioner (såsom barn med hiv-infektion, sicklecellanemi eller nedsatt eller onormal mjältfunktion) kan få Synflorix. Fråga läkaren hur många injektioner ditt barn ska få och när de ska ges.
Om ditt barn missar en injektion är det viktigt att du får en ny tid. Detta så att du och din läkare kan prata om vad som bör göras härnäst för att skydda ditt barn.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare, apotekspersonal eller sjuksköterska.
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem. Följande biverkningar kan förekomma med detta läkemedel:
Allvarliga allergiska reaktioner kan förekomma i mycket sällsynta fall (vid upp till 1 av 10 000 vaccindoser). Sådana reaktioner känns igen genom:
upphöjda och kliande utslag (nässelutslag)
svullnad, ibland av ansikte och mun (angioödem), som orsakar andningssvårigheter
kollaps.
Dessa reaktioner inträffar normalt innan man lämnat läkarmottagningen. Om ditt barn får något av dessa symtom, kontakta omedelbart läkare.
Mycket vanliga (dessa kan förekomma vid fler än 1 av 10 vaccindoser)
smärta, rodnad eller svullnad där injektionen ges
feber, 38°C eller högre
sömnighetskänsla
irritationskänsla
aptitlöshet.
Vanliga (dessa kan förekomma vid upp till 1 av 10 vaccindoser)
förhårdnad vid injektionsstället.
Mindre vanliga (dessa kan förekomma vid upp till 1 av 100 vaccindoser)
klåda, blåmärken, blödning eller en liten knöl där injektionen har getts
illamående, diarré eller kräkning
ihållande gråt
tillfälligt andningsuppehåll (apné) om ditt barn är för tidigt fött (före eller i 28:e graviditetsveckan)
huvudvärk
hudutslag
diffus svullnad av den injicerade kroppsdelen, som ibland även innefattar närliggande led
nässelfeber.
Sällsynta (dessa kan förekomma vid upp till 1 av 1 000 vaccindoser)
krampanfall utan feber eller på grund av hög feber
allergiska reaktioner t.ex. hudallergier
kollaps (plötslig debut av muskelslapphet), perioder av medvetslöshet eller nedsatt medvetande samt blekhet eller blåaktig missfärgning av huden.
Mycket sällsynta (dessa kan förekomma vid upp till 1 av 10 000 vaccindoser)
Kawasakis sjukdom (främsta tecknen på sjukdomen är t.ex. feber, hudutslag, svullna lymfkörtlar, inflammation och utslag på slemhinnorna i mun och hals).
Boosterdoser av Synflorix kan öka risken för biverkningar.
För barn >12 månaders ålder kan risken för smärta vid injektionsstället öka med ökad ålder.
Hos mycket för tidigt födda barn (födda i graviditetsvecka 28 eller tidigare) kan det förekomma längre uppehåll mellan andetagen än normalt under 2-3 dagar efter vaccination.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera eventuella biverkningar direkt till Läkemedelsverket, www.lakemedelsverket.se. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Läkemedelsverket
Box 26
751 03 Uppsala
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 °C‑8 °C).
Förvaras i originalförpackningen. Ljuskänsligt.
Får ej frysas.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
De aktiva substanserna är: En dos på 0,5 ml innehåller: | ||
Pneumokockpolysackarid serotyp 11,2 | 1 mikrogram | |
Pneumokockpolysackarid serotyp 41,2 | 3 mikrogram | |
Pneumokockpolysackarid serotyp 51,2 | 1 mikrogram | |
Pneumokockpolysackarid serotyp 6B1,2 | 1 mikrogram | |
Pneumokockpolysackarid serotyp 7F1,2 | 1 mikrogram | |
Pneumokockpolysackarid serotyp 9V1,2 | 1 mikrogram | |
Pneumokockpolysackarid serotyp 141,2 | 1 mikrogram | |
Pneumokockpolysackarid serotyp 18C1,3 | 3 mikrogram | |
Pneumokockpolysackarid serotyp 19F1,4 | 3 mikrogram | |
Pneumokockpolysackarid serotyp 23F1,2 | 1 mikrogram | |
1 adsorberat på aluminiumfosfat | totalt 0,5 milligram Al3+ | |
2 konjugerat till protein D (härstammande från icke-typningsbara Haemophilus influenzae) bärarprotein | 9-16 mikrogram | |
3 konjugerat till tetanustoxoid-bärarprotein | 5-10 mikrogram | |
4 konjugerat till difteritoxoid-bärarprotein | 3-6 mikrogram | |
Övriga innehållsämnen är: natriumklorid (se avsnitt 2 för mer information) och vatten för injektionsvätskor | ||
Injektionsvätska, suspension i förfylld spruta.
Synflorix är en grumlig vit suspension.
Synflorix finns som förfyllda sprutor för 1 dos med eller utan nål i förpackningar om 1, 10 eller 50.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Belgien
För ytterligare upplysningar om detta läkemedel, kontakta ombudet för innehavaren av godkännandet för försäljning:
Belgique/België/Belgien GlaxoSmithKline Pharmaceuticals s.a./n.v. Tél/Tel: + 32 10 85 52 00 | Lietuva GlaxoSmithKline Biologicals SA Tel: +370 80000334 |
България GlaxoSmithKline Biologicals SA Тел.: + 359 80018205 | Luxembourg/Luxemburg GlaxoSmithKline Pharmaceuticals s.a./n.v. Tél/Tel: + 32 10 85 52 00 |
Česká republika GlaxoSmithKline s.r.o. Tel: + 420 2 22 00 11 11 cz.info@gsk.com | Magyarország GlaxoSmithKline Biologicals SA Tel.: + 36 80088309 |
Danmark GlaxoSmithKline Pharma A/S Tlf: + 45 36 35 91 00 dk-info@gsk.com | Malta GlaxoSmithKline Biologicals SA Tel: + 356 80065004 |
Deutschland GlaxoSmithKline GmbH & Co. KG Tel: + 49 (0)89 360448701 produkt.info@gsk.com | Nederland GlaxoSmithKline BV Tel: + 31 (0)33 2081100 |
Eesti GlaxoSmithKline Biologicals SA Tel: +372 8002640 | Norge GlaxoSmithKline AS Tlf: + 47 22 70 20 00 |
Ελλάδα GlaxoSmithKline Μονοπρόσωπη A.E.B.E Tηλ: + 30 210 68 82 100 | Österreich GlaxoSmithKline Pharma GmbH. Tel: + 43 (0)1 97075 0 at.info@gsk.com |
España GlaxoSmithKline, S.A. Tel: + 34 900 202 700 es-ci@gsk.com | Polska GSK Services Sp. z o.o. Tel.: + 48 (22) 576 9000 |
France Laboratoire GlaxoSmithKline Tél: + 33 (0) 1 39 17 84 44 diam@gsk.com | Portugal GlaxoSmithKline - Produtos Farmacêuticos, Lda. Tel: + 351 21 412 95 00 FI.PT@gsk.com |
Hrvatska GlaxoSmithKline Biologicals SA Tel.: + 385 800787089 | România GlaxoSmithKline Biologicals SA Tel: +40 800672524 |
Ireland GlaxoSmithKline (Ireland) Ltd Tel: + 353 (0)1 4955000 | Slovenija GlaxoSmithKline Biologicals SA Tel: + 386 80688869 |
Ísland Vistor hf. Sími: +354 535 7000 | Slovenská republika GlaxoSmithKline Biologicals SA Tel: + 421 800500589 |
Italia GlaxoSmithKline S.p.A. Tel:+ 39 (0)45 7741 111 | Suomi/Finland GlaxoSmithKline Oy Puh/Tel: + 358 10 30 30 30 |
Κύπρος GlaxoSmithKline Biologicals SA Τηλ: + 357 80070017 | Sverige GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 info.produkt@gsk.com |
Latvija GlaxoSmithKline Biologicals SA Tel: + 371 80205045 | United Kingdom (Northern Ireland) GlaxoSmithKline Biologicals SA Tel: +44 (0)800 221 441 customercontactuk@gsk.com |
Denna bipacksedel ändrades senast: 2021-09-16
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats: http://www.ema.europa.eu/
En fin vit bottensats med en klar färglös supernatant kan iakttas vid förvaring av den förfyllda sprutan. Detta utgör inget tecken på försämring.
Före administrering ska innehållet i den förfyllda sprutan inspekteras visuellt både före och efter omskakning med avseende på främmande partiklar och/eller utseendemässiga förändringar. Om något av detta iakttas ska vaccinet kasseras.
Vaccinet bör uppnå rumstemperatur före användning.
Vaccinet ska omskakas väl före användning.
Vaccinet ska endast ges intramuskulärt. Administrera det inte intravaskulärt.
Om Synflorix ges samtidigt som andra vacciner ska olika injektionsställen användas.
Synflorix ska inte blandas med andra vacciner.
Instruktioner för administrering av vaccin i förfyllda sprutor
1. | Håll sprutcylindern i en hand (undvik att hålla i kolvstången) och skruva av skyddslocket på sprutan genom att vrida det motsols. | 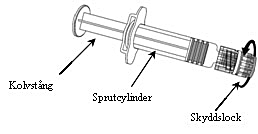 |
2 | För att fästa nålen på sprutan, skruva nålen medsols in i sprutan tills den låser sig. | 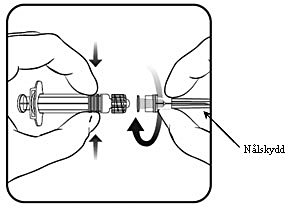 |
3. | Ta bort nålskyddet, som i vissa fall kan sitta lite hårt. |
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.